Линко
Новая платформаЛинко
Скрыть менюГлавная
Поиск. Обзор сервисов Назад в раздел
Статьи по данной теме


В этой статье мы поговорим об особенностях вступления в силу Критериев аккредитации, об изменениях к документу, рассмотрим структуру, группы лабораторий и разделение требований к ним, определимся с общими и дополнительными требованиями, упомянем ссылочные стандарты, поговорим о подтверждении опыта персонала, ответим на популярные вопросы по теме и рассмотрим перечень документов, необходимых для подтверждения соответствия критериям аккредитации.
Вводное слово
Утверждение новых критериев
Изменения к приказу № 707
Структура
Ссылочные материалы критериев
Классификация лабораторий
Общие требования (п. 21)
Аккредитация медицинских лабораторий – новинка
Перечень документов по стандартизации
Дополнительные требования
Требования к персоналу
Сотрудники, не отвечающие критериям
«Покрытие» области аккредитации персоналом
Занятость сотрудников в нескольких лабораториях
Общие требования к материальным ресурсам
Исследования и измерения по месту осуществления временных работ
Требование к помещениям
Требования к нормативной документации
Требования к управлению документацией лаборатории
Документы, подтверждающие соответствие критериям
Использование знака национальной системы аккредитации
Подтверждение опыта сотрудника
Предоставление сведений о лаборатории
Идентификация помещений
В этой статье мы поговорим об особенностях вступления в силу Критериев аккредитации, об изменениях к документу, рассмотрим структуру, группы лабораторий и разделение требований к ним, определимся с общими и дополнительными требованиями, упомянем ссылочные стандарты, поговорим о подтверждении опыта персонала, ответим на популярные вопросы по теме и рассмотрим перечень документов, необходимых для подтверждения соответствия критериям аккредитации.
Критерии аккредитации действуют вот уже более трех месяцев. Они просты в понимании и их не так много, как было в предыдущей версии документа. Однако, мы видим, что у многих лабораторий остаются одни и те же вопросы, касающиеся персонала, права владения помещениями и оборудованием, и другие вопросы. Некоторые моменты все еще непонятны и даже неверно толкуются, в некоторых вопросах принимаются решения с целью перестраховки. Поэтому мы хотим подытожить рассуждения по этим вопросам, обратить на них особое внимание в статье и отметить правильный вариант действий.
Критерии аккредитации, утвержденные приказом Минэкономразвития от 26 октября 2020 года № 707, заменяют критерии аккредитации, установленные приказом № 326, которые действовали по 2020 год.
Критерии устанавливают требования, которым должны удовлетворять заявитель и аккредитованные в национальной системе аккредитации лица для осуществления своей деятельности в области аккредитации.
Критерии аккредитации и перечень документов, подтверждающих соответствие заявителя, аккредитованного лица критериям аккредитации, вступили в силу с 1 января 2021 года за исключением некоторых положений, которые вступают в силу с 1 июля 2021 года и с 1 января 2022 года.
Некоторые требования в данных критериях не применяются в отношении лиц, уже аккредитованных на дату вступления критериев в силу, и заявителей до 1 июля 2021 года.
На схеме далее отмечено, когда и какие требования Критериев аккредитации и требования связанных с ними документов по стандартизации вступают в силу.
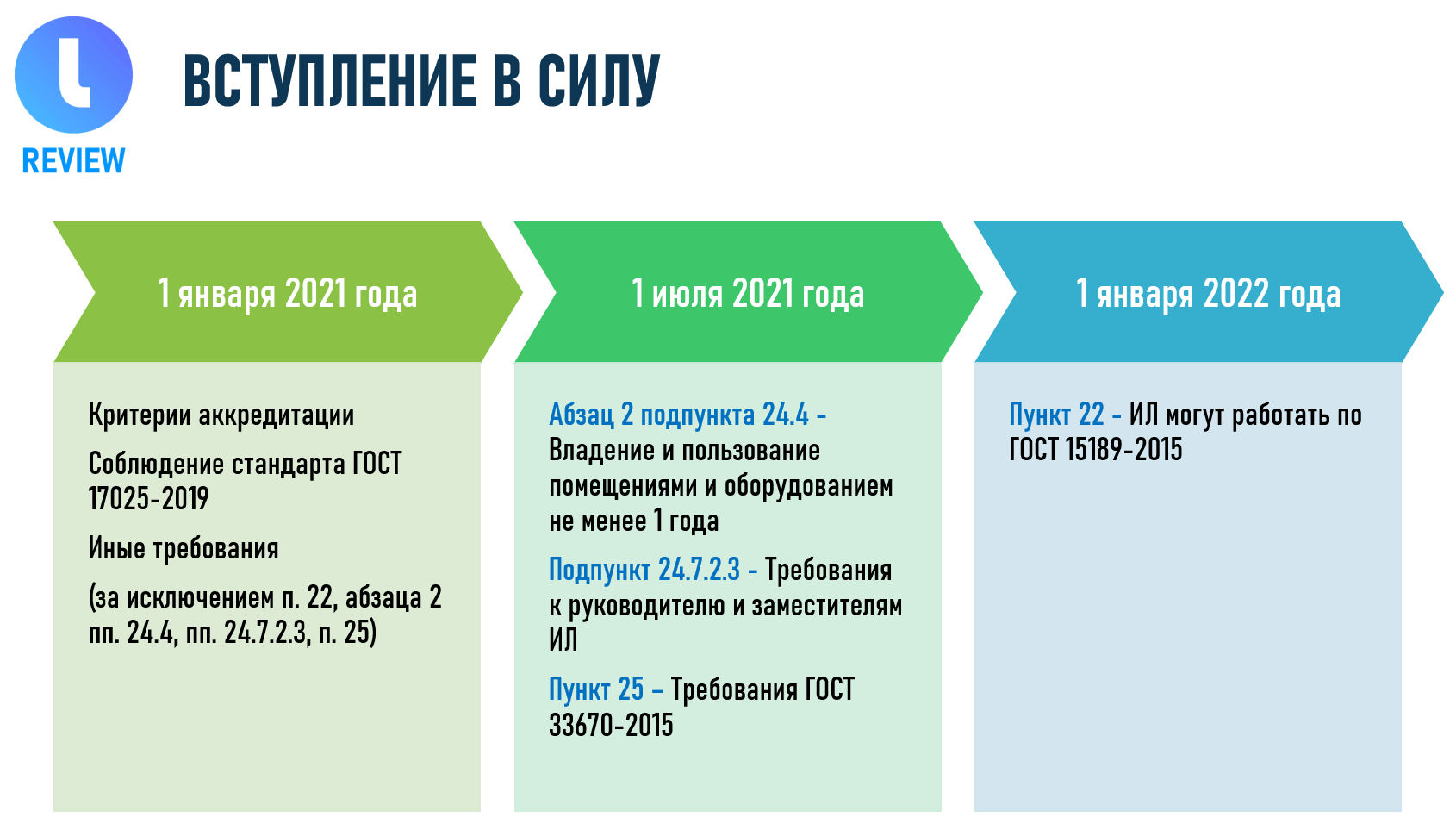
30 декабря 2020 года были приняты изменения к приказу, утверждающему критерии аккредитации. Данные изменения устраняют опечатки, допущенные при редактировании проекта, которые попали в первую версию документа.
Что было принято данными изменениями?
Исправлены некорректные ссылки на несуществующие абзацы пунктов.
Исправлены несвязанные с определенными разделами критериев ссылки, в частности в пункте 39, который касается лиц, выполняющих работы и оказывающих услуги по обеспечению единства измерений. Загадочное число 28 было заменено на слова «пункт 46» о требовании к разработке документа системы менеджмента. В целом, устранены ошибки, связанные с некачественным редактированием проекта документа.
Документ стал более удобным. Критерии аккредитации структурированы по типам аккредитованных лиц, поэтому будет очень просто работать с этим документом. В отдельный блок сгруппированы общие и дополнительные требования к лабораториям, а также выделен блок с документами, подтверждающими соответствие критериям аккредитации.
Если обратиться к странице, на которой размещены действующие критерии аккредитации на платформе, то помимо хорошей структуры, Вы найдете:
Страница позволяет осуществлять поиск по тексту (комбинацией клавиш Ctrl+F), что очень удобно, когда нужно найти небольшую фразу из контекста. Это является большим преимуществом перед бумажной версией. Также документ всегда находится под рукой. Для этого в браузере необходимо добавить его себе на панель избранных закладок.
И главной особенностью является наличие выпадающих комментариев по тексту критериев. В них вы найдете то, о чем мы будем говорить в этой статье.
В приложении к критериям можно найти все ссылки на национальные стандарты и документы международных организаций в области аккредитации.
Важными ссылочными документами для лабораторий являются:
Из новых документов здесь появляются только требования «Правил к оформлению протоколов испытаний». Но и этот документ очень близок к тем требованиям, которые предъявляются к отчетам о результатах, и определены в ГОСТ ISO/IEC 17025-2019.
Исходя из видов деятельности и области применения результатов лабораторной деятельности, все лаборатории разделяются на 3 группы:
1. Лаборатории, выполняющие работы по исследованиям и испытаниям, измерениям в целях обязательного подтверждения (оценки) соответствия. Например, проводящие работы по специальной оценке условий труда (СОУТ). Лаборатории, которые проводит испытания на соответствие техническим регламентам.
2. Лаборатории, в отношении которых законодательством России установлены требования по наличию аккредитации в национальной системе аккредитации. Для того, чтобы определить, относится ли Ваша лаборатория к данной группе необходимо изучить законодательство в области деятельности вашей лаборатории, организации.
3. Остальные лаборатории.
В соответствии с той группой, к которой относится лаборатория, на нее распространяются требования конкретных пунктов критериев аккредитации.
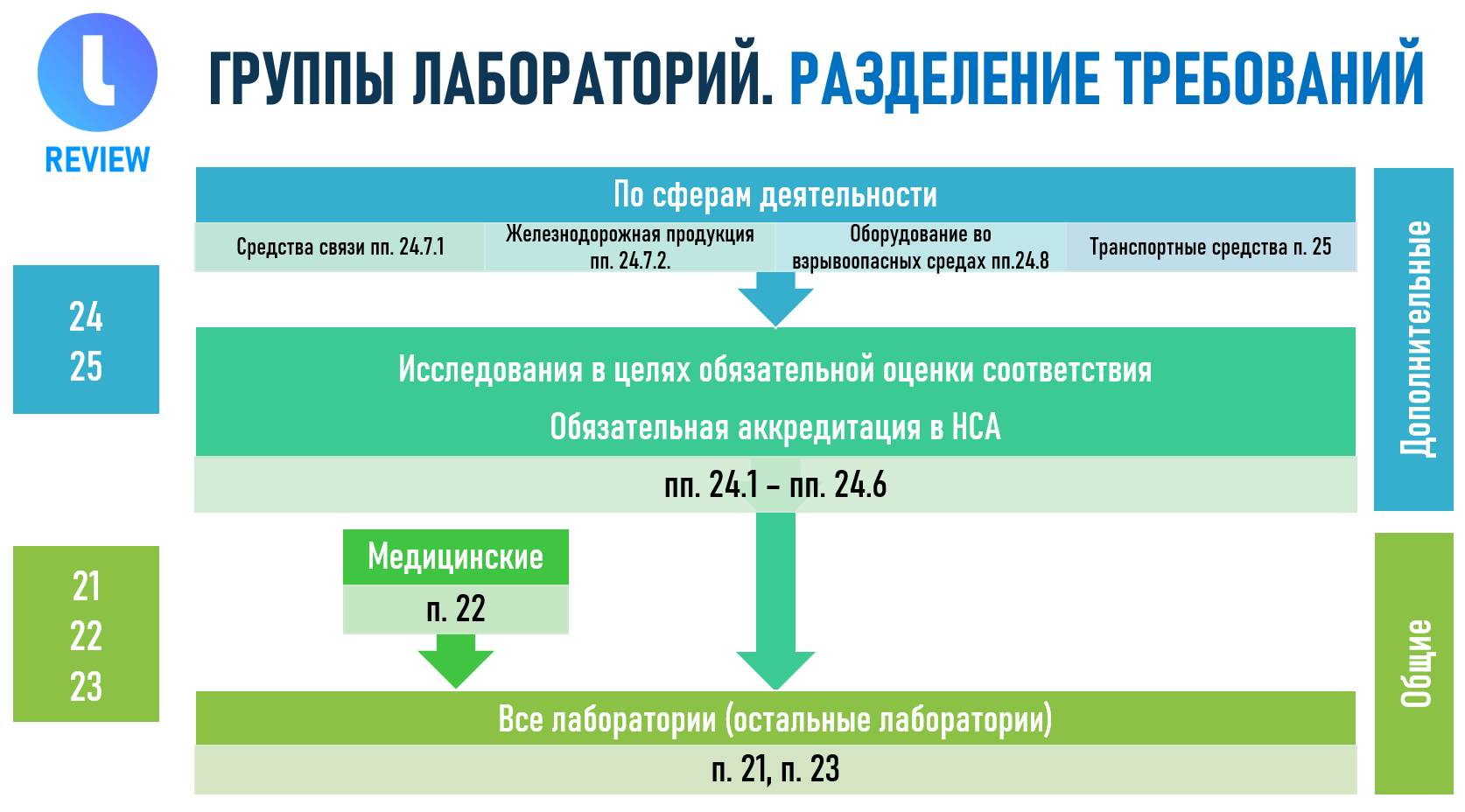
Пункты 21, 23 критериев аккредитации должны выполняться всеми испытательными лабораториями.
Лаборатории, выполняющие испытания в целях обязательного подтверждения (оценки) соответствия, а также те, в отношении которых законодательством установлены требования по наличию аккредитации в национальной системе аккредитации, дополнительно эти лаборатории должны выполнять помимо пунктов 21 и 23 требования подпунктов с 24.1 по 24.6.
В критериях также выделены требования для испытательных лабораторий по различным сферам деятельности:
На лабораториях, разделенных по сферам деятельности в рамках статьи мы не будем подробно останавливаться.
Общие требования относятся ко всем испытательным лабораториям.
В общих требованиях определены документы, требования которых должны выполнять все лаборатории.
Главным требованием к лабораториям является то, что лаборатория должна соответствовать требованиям, установленным положениями стандарта ГОСТ ISO/IEC 17025-2019 «Общие требования к компетентности испытательных и калибровочных лабораторий».
Одна из новинок критериев касается лабораторий, проводящих биологические, микробиологические, иммунологические или другие исследования материалов из организма человека (п. 22).
Критериями определено, что для таких лабораторий вместо стандарта ГОСТ ISO/IEC 17025-2019 можно применять требования, установленные положениями ГОСТ Р ИСО 15189-2015 «Лаборатории медицинские. Частные требования к качеству и компетентности».
Этот пункт вступает в силу с 1 января 2022 года.
С точки зрения терминологии данный стандарт более адаптирован для лабораторий, осуществляющих эти виды исследований материалов из организма человека. Ну и в связи с включением данного пункта в критерии аккредитации, Росаккредитация получила эксклюзивные полномочия осуществлять аккредитацию медицинских лабораторий на соответствие данному стандарту.
Перечень документов по стандартизации, требования которых должна выполнять лаборатория, представлен в п. 23.
В список вошли: «Политика ИЛАК по прослеживаемости результатов измерений», «Политика ИЛАК в отношении неопределенности при калибровках». Требование соблюдать данные политики перешло в «общие требования» из приложения №2 к Приказу № 326.
Признание результатов исследований (испытаний) и измерений участников национальной системы аккредитации подразумевает соблюдение настоящих политик ИЛАК в отношении прослеживаемости результатов измерений и неопределенности при калибровках.
ГОСТ Р 58973-2020 «Правила к оформлению протоколов испытаний», вступает в силу с 1 июля 2021 года. Правила являются еще одной новинкой действующих критериев аккредитации для лабораторий. Требования настоящего стандарта очень близки к требованиям, определенным в ГОСТ ISO/IEC 17025-2019.
Часто лаборатории задают вопрос:
Должен ли применяться стандарт ГОСТ Р 58973-2020 как обязательный документ для лабораторий, которые проводят измерения, испытания в добровольной сфере?
Ответ: да, должен. С 1 июля 2021 года. Это требование общее, а общие требования должны выполняться всеми заявителями и лицами, аккредитованными в национальной системе аккредитации.
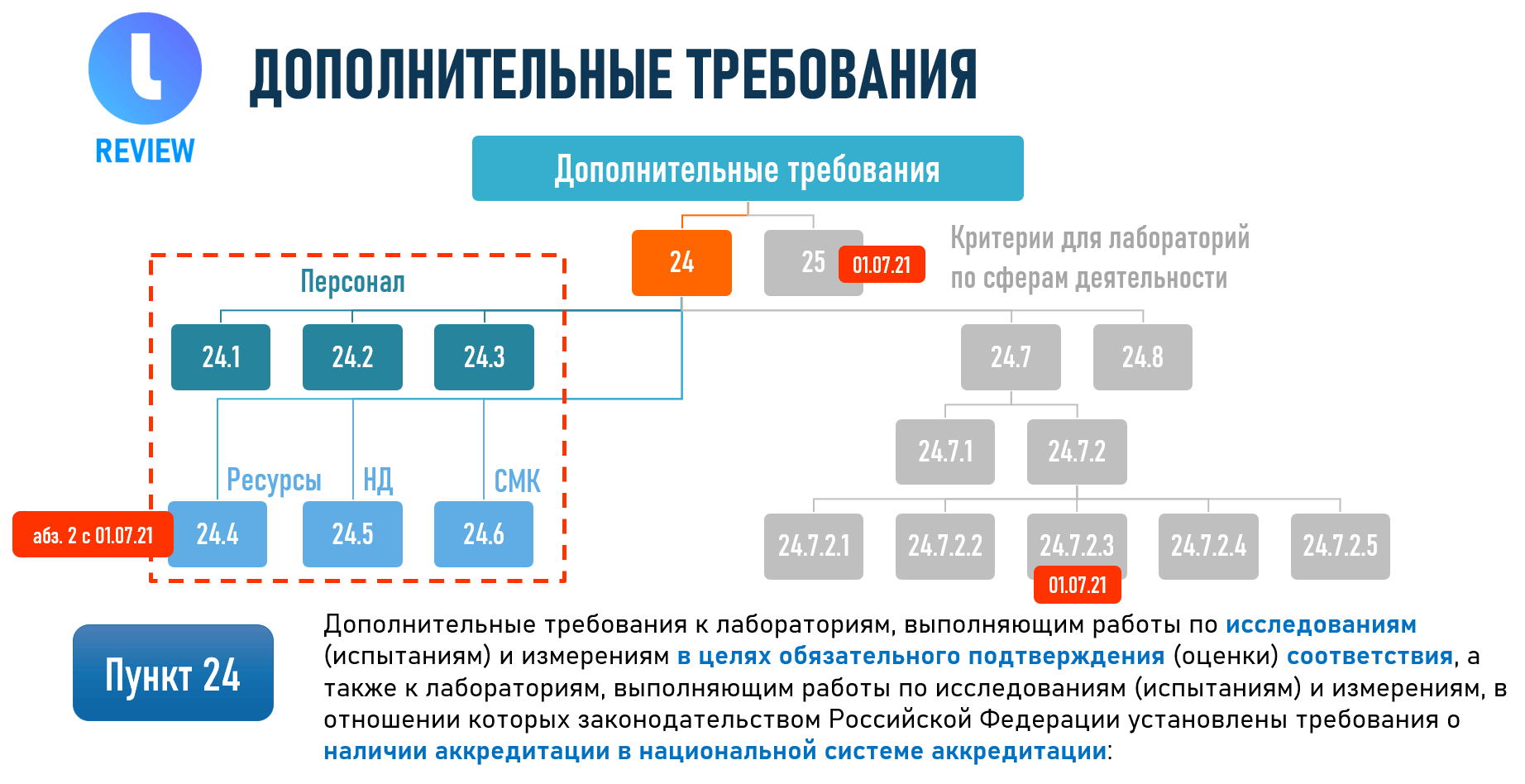
В отношении лабораторий, выполняющих работы по исследованиям (испытаниям) и измерениям в целях обязательного подтверждения (оценки) соответствия, а также лабораторий, исполняющих работы, в отношении которых законодательством России установлено требование о наличии аккредитации в национальной системе аккредитации, установлены дополнительные требования (п. 24).
Также существуют дополнительные требования к лабораториям, осуществляющим оценку соответствия определенных объектов (проводящим сертификационные испытания средств связи, выполняющим работы по исследованиям железнодорожной продукции, оборудования для работы во взрывоопасных средах, проводящим проверку выполнения требований к единичным транспортным средствам).
Все дополнительные требования к таким лабораториям вынесены в отдельные пункты критериев аккредитации.
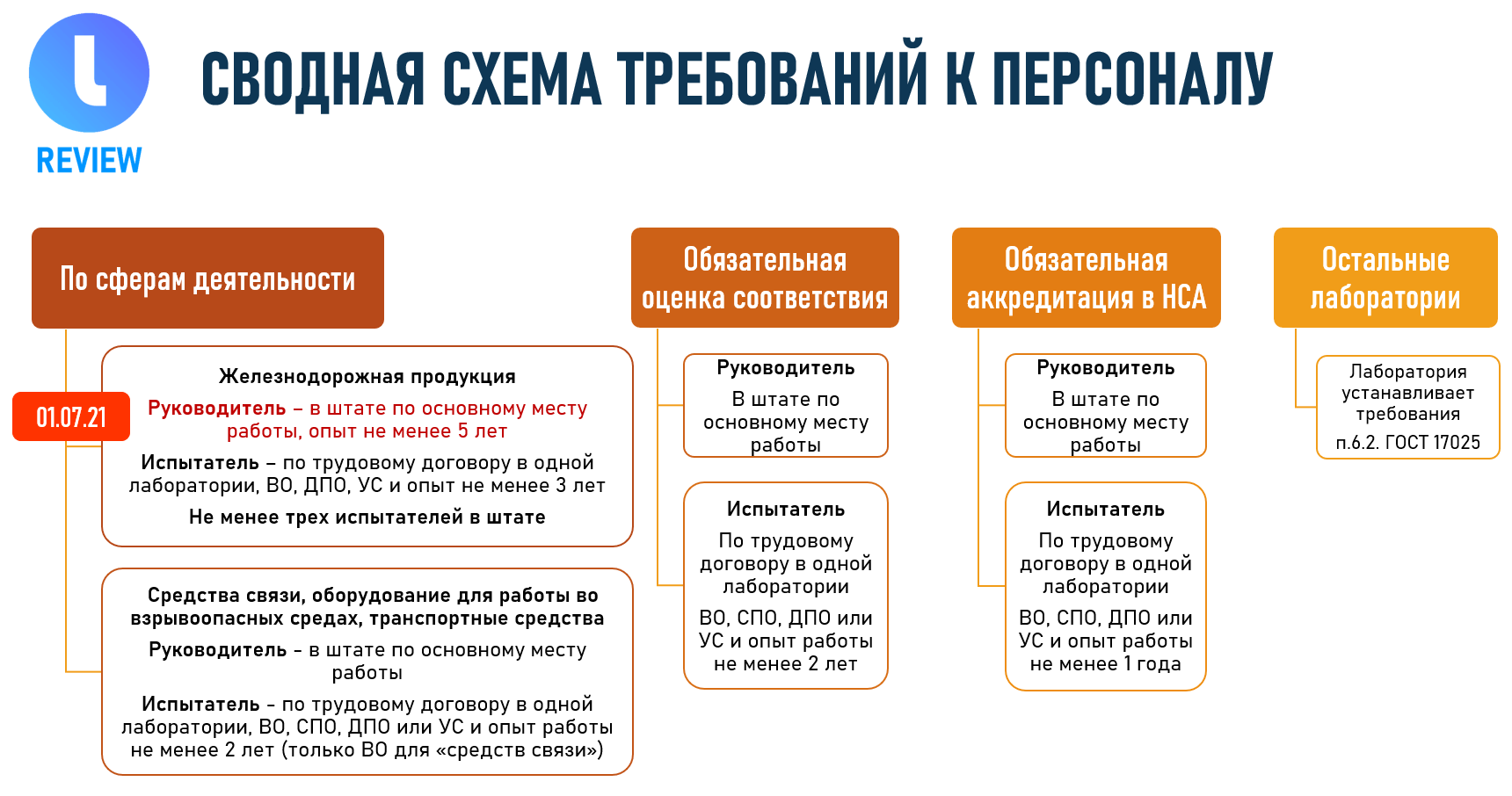
В соответствии с разделением лабораторий на группы существенно изменились требования к персоналу.
Для лабораторий, выполняющих работы в целях обязательного подтверждения (оценки) соответствия, опыт работы персонала, осуществляющего исследования, должен быть не менее 2 лет. Ранее было 3 года, теперь только 2 года. Если сотрудник на день вступления в силу критериев аккредитации имел опыт работы 2 года, то такой сотрудник может получить допуск к самостоятельному выполнению исследования.
Для лабораторий, выполняющих работы, в отношении которых установлены требования о наличии аккредитации в национальной системе аккредитации, опыт работы персонала должен быть не менее одного года.
Как и в случае с лабораториями, выполняющими работы в целях обязательного подтверждения (оценки) соответствия, если сотрудник на день вступления в силу критериев аккредитации имел опыт работы равный одному году, то такой сотрудник может получить допуск к самостоятельному выполнению исследований.
Для остальных лабораторий требования к опыту работы персонала критериями не определены. Нет требований к опыту работы. Поэтому важно будет подтвердить компетентность и навыки персонала при аккредитации или при прохождении процедуры подтверждения компетентности. Это является существенным изменением и большим шагом в сторону выполнения требований стандарта ГОСТ ISO/IEC 17025-2019, где мы видели требования об оценке, мониторинге компетентности персонала. Лабораториям необходимо самостоятельно принять правила допуска персонала к работе по исследования.
В отношении лабораторий, осуществляющих контроль железнодорожной продукции, требование к опыту работы сохранилось и составляет 3 года.
Требования к образованию сотрудников, проводящих испытания, в сравнении с предыдущим приказом не изменились: высшее, среднее профессиональное, дополнительное профессиональное образование или ученая степень по специальности или направлению подготовки соответствующей области аккредитации (п. 24.1).
Допускается привлечение к исследованиям сотрудников, не отвечающих критериям аккредитации, указанным ранее, за исключением подписания протоколов испытаний и иных документов, содержащих результаты испытаний и измерений, при условии выполнении работ по испытаниям под контролем лиц, отвечающих требованиям настоящего пункта критериев аккредитации (п. 24.1).
Рабочие записи, не являющиеся итоговыми документами, не содержащие результаты испытаний, могут быть подписаны сотрудником, не отвечающим критериям аккредитации, но при этом должно быть зафиксировано и подтверждено подписью, что эти работы выполнялись под контролем сотрудника, отвечающего критериям аккредитации.
Таким образом, условия привлечения к выполнению работ лиц, не отвечающих требованиям критериев, в отличие от предыдущей версии критериев аккредитации не изменились.
Работниками лаборатории, непосредственно выполняющими работы, состоящими в штате по основному месту работы, должно обеспечиваться проведение исследований, испытаний и измерений по не менее чем половине включенных в область аккредитации стандартов, содержащих правила, методы исследования, в том числе правила отбора образцов, необходимые для применения и исполнения требований, принятых технических регламентов, и осуществления оценки подтверждения соответствия продукции.
Разумеется, здесь речь идет обо всех документах, содержащих правила и методы исследований, а не только о стандартах.
Работник лаборатории, непосредственно выполняющий работы по исследованиям, испытаниям и измерениям в области аккредитации, может работать по трудовому договору в составе только одной лаборатории.
Несколько распространенных вопросов от лабораторий в отношении данного абзаца критериев:
Может ли работник, непосредственно проводящий исследования (испытания), измерения, быть оформлен в аккредитованной лаборатории по договору совместительства?
Ответ: может. Работники, которые непосредственно выполняют работы по исследованиям (испытаниям), измерениям, могут быть оформлены в аккредитованной лаборатории по трудовому договору по основному месту работы или по трудовому договору на выполнение работ по внешнему или внутреннему совместительству.
Может ли работник, непосредственно проводящий исследования, быть оформлен в аккредитованной лаборатории, выполняющей работы по исследованиям в целях обязательного подтверждения (оценки) соответствия и также выполнять работы по договору ГПХ (гражданско-правового характера) по исследованиям, в отношении которых в законодательстве установлены обязательные требования по аккредитации в национальной системе аккредитации?
Ответ: нет, не может. Исходя из требований абзаца 2 подпункта 24.2 критериев, работники лаборатории, которые непосредственно выполняют работы по исследованиям и измерениям в области аккредитации, могут работать только по трудовому договору.
Может ли работник аккредитованной лаборатории, выполняющий работы по исследованиям в целях обязательного подтверждения оценки соответствия, работать в другой лаборатории?
Ответ: Абзацем вторым пункта 24.2 установлено, что работник, непосредственно выполняющий работы по исследованиям (испытаниям), измерениям, может работать по трудовому договору в составе только одной лаборатории.
Таким образом, для работников, которые осуществляют данную деятельность по основному месту работы, местом работы по совместительству не может являться другая аккредитованная лаборатория. Также для работников, осуществляющих данную деятельность по договору совместительства, основным местом работы не может являться другая аккредитованная лаборатория.
Вместе с тем, работник, который выполняет работы по исследованиям в аккредитованной лаборатории, может осуществлять свою деятельность в другой аккредитованной лаборатории, ну а тем более в неаккредитованной лаборатории, однако при этом он должен выполнять деятельность, которая не связана с работой по исследованиям и испытаниям, отбору образцов.
Работа сотрудников по совместительству в разных лабораториях это риск для лабораторий. Риск возникновения таких ситуаций, безусловно, должен быть рассмотрен и оценен лабораториями.
Руководитель лаборатории и его заместители должны работать в штате лаборатории по основному месту работы.
Данный пункт не разрешает руководителю работать на должности руководителя лаборатории по совместительству, трудовому соглашению.
Но не запрещается руководителю работать в различных лабораториях. Данный пункт устанавливает, что руководитель должен быть именно в штате лаборатории по основному месту работы. При этом руководитель может выполнять работы в других организациях.
Может ли руководитель или заместитель руководителя лаборатории выполнять исследования, испытания, измерения?
Критериями аккредитации не установлен запрет на выполнение работ по исследованиям руководителем и заместителем руководителя.
Абзацем третьим подпункта 24.2 критериев установлено, что руководитель либо его заместители, которые выполняют работы в целях обязательного подтверждения оценки соответствия, а также выполняют работы по испытаниям, измерениям, в отношении которых законодательством РФ установлено обязательное требование по аккредитации в национальной системе аккредитации, должны работать в штате по основному месту работ. Вместе с этим выполнять работы по исследованиям, измерениям руководители лабораторий могут только по договору совместительства либо внутреннего, либо внешнего.
Общие требования к материальным ресурсам, которыми должна располагать лаборатория, формально не изменились, однако появились отдельные конкретные требования. Также в отдельную группу выделены государственные и муниципальные учреждения.
Следующие требования распространяется только на лаборатории, которые прошли процедуру аккредитации после вступления в силу новых критериев аккредитации после 1 января 2021.
Право владения и пользования помещениями, испытательным оборудованием, средствами измерений не может быть приобретено на срок менее одного года за исключением двух случаев:
1. Оборудование, не имеющее широкого распространения, не требующее регулярного обслуживания (уникальное оборудование), которое находится по месту его применения и используется на праве собственности или на ином законном основании, предусматривающем право пользования.
2. Испытания железнодорожной продукции.
Данный пункт действует с 1 июля 2021 года.
Подпунктом 24.4 для государственных и муниципальных учреждений допускаются определенные требования о наличии по месту осуществления деятельности в области аккредитации помещений, оборудования, стандартных образцов на ином законном основании, предусматривающем право пользования.
Какие документы подтверждают право владения и использования материально-технических средств, оборудования и помещений?
Для помещений это выписка из реестра по недвижимости, если отсутствует свидетельство о государственной регистрации права на помещения. Для оборудования и иных средств в качестве подтверждения может быть использован любой бухгалтерский документ, который свидетельствует о праве владения и использования: оборотно-сальдовая ведомость, инвентаризационная опись и иные бухгалтерские документы. Счёт в данном случае не подтверждает право владения и использования.
Требования к проведению исследований (испытаний) и измерений по месту осуществления временных работ.
Лаборатория может проводить испытания по месту осуществления временных работ в случае, если работы по испытаниям проводятся за пределами места осуществления деятельности лаборатории, но с использованием оборудования, а также иных технических средств и материальных ресурсов, указанных в абзацах 1-3 подпункта 24.4. То есть используемых на законных основаниях с правом владения и пользования.
Это касается тех лабораторий, которые, например проводят испытания непосредственно у заказчика.
Интересное требование есть в отношении помещений.
Помещения для проведения работ по исследованиям, [испытаниям, измерениям] по производственной площади, характеру и объему выполняемых работ должны соответствовать требованиям документов по исследованиям, испытаниям и измерениям, инструкций по эксплуатации оборудования при наличии таких требований.
Разумеется, под этим понимаются требования любой эксплуатационной документации, как бы она не называлась: инструкция, руководство, паспорт и другие. Очень внимательно стоит изучить или вспомнить требования к помещениям, особенно при установке оборудования в помещениях, потому что сейчас задан тренд в этом направлении. Более того, у Вас появляется дополнительная, отличная возможность к обоснованию перед руководством организации расширения помещений лаборатории, ремонта, реконструкции помещений. Всё-таки изменения такого уровня происходят редко и важно успеть этим воспользоваться, если у Вас еще есть над чем работать.
В отдельный пункт критериев выделено требование к обеспечению лаборатории нормативно-правовыми актами и иными документами.
Требование данного пункта заключается в том, что лаборатория должна располагать нормативными правовыми актами, документами по стандартизации, правилами и методами исследований (испытаний) и измерений, в том числе правилами отбора образцов проб, иными документами, указанными в области аккредитации, заявлении об аккредитации или в реестре аккредитованных лиц, а также соблюдать требования данных документов (п. 24.5).
Как мы видим, ничего нового в данном требовании нет. Данное требование аналогично указанному в ГОСТ ISO/IEC 17025-2019, однако требования ГОСТа, как и в части оборудования и помещений, являются более внятными.
Документ СМК лаборатории должен включать систему управления документацией (правила документооборота), которая должна регламентировать:
1. Правила резервного копирования и восстановления документов.
2. Систему хранения и архивирования документов, том числе правила хранения и архивирования, предусматривающие хранение на бумажных носителях и (или) в форме электронных документов, подписанных усиленной квалифицированной подписью, по месту (местам) осуществления деятельности в области аккредитации архива документов, в том числе документов, представленных в лабораторию заявителями для проведения исследований (испытаний) и измерений, в течение 3 лет со дня выдачи соответствующего документа о результатах исследований (испытаний) и измерений, или принятия решений об отказе в его выдаче.
3. Правила систематизации и ведения архива документов, в том числе условия передачи документов в архив, условия выдачи документов из архива, сроки хранения в архиве документов (групп документов), правила регистрации документов, поступающих в архив, условия хранения документов.
Данные требования переехали из предыдущей версии критериев аккредитации (пункта 23.7). Все остальные требования входят в состав стандарта ГОСТ ISO/IEC 17025/2019.
Исчезло требование к Руководству по качеству. Предполагается, что лаборатория разрабатывает набор документов или один документ. Таким документом может остаться Руководство по качеству.
Важно обратить внимание на то, что данный пункт требует наличие не резервного копирования и восстановления документов, а ПРАВИЛ резервного копирования и восстановления. Резервное копирование должно помогать восстанавливать документы в случае их потери. Нет обязательного требования копировать все. Должны быть установлены только правила: что копировать, что делать, если необходимо восстановить какой-либо документ. Сегодня на фоне неоднозначных требований разыгралось множество спекуляций по данному вопросу. Статья «Резервное копирование документов в лаборатории» разъясняет один из подходов к этому вопросу с точки зрения оценки рисков.
Критериями установлен минимальный срок хранения протоколов до 3 лет со дня выдачи документа. Документами на конкретные виды продукции может быть определен иной период хранения протоколов.
Теперь рассмотрим документы и сведения, подтверждающие соответствие лабораторий (испытательных и калибровочных) критериям аккредитации:
документ (документы) системы менеджмента качества, содержащие требования системы менеджмента качества лаборатории в соответствии с настоящими критериями аккредитации, в том числе правила применения изображения знака национальной системы аккредитации.
Данное требование подразумевает разработку положений системы менеджмента качества в соответствии с требованиями ГОСТ ISO/IEC 17025-2019. Система менеджмента качества должна быть разработана в соответствии с требованиями этого ГОСТа ISO/IEC 17025-2019 или должна быть интегрирована в систему менеджмента организации и соответствовать требованиям стандарта ISO 9001. Дополнительные требования к системе менеджмента изложены в стандарте ГОСТ ISO/IEC 17025-2019.
Что делать, если лаборатория не применяет и не заявляет об использовании изображения знака национальной системы аккредитации? В Руководстве по качеству достаточно написать, что вы не используете знак национальной системы аккредитации. В этом случае дополнительных правил его использования указывать не требуется. Однако, на практике взгляды экспертов в данном вопросе не обоснованно расходятся.
Как подтвердить опыт сотрудников? Этот вопрос уже многократно обсуждался. И самые очевидные ответы таковы, что лучше всего опыт подтверждается записями в трудовой книжке, в том числе электронной, копиями должностной инструкции с предыдущих мест работы. Однако, в трудовой книжке нет записей о том, в какой области аккредитации работал сотрудник и какие исследования выполнял, и в должностной инструкции очень редко фиксируется данная информация.
Хорошим способом подтвердить опыт будет предоставление сведений о лаборатории, где указана область деятельности, в которой работал сотрудник, или выписки этой информации с предыдущего места работы. Забота о подтверждении опыта сотрудников сегодня ложится на плечи не только аккредитованных лиц, но и на самих сотрудников лаборатории.
Вместе с тем, хотелось бы отметить подпункт 26.2, где в документах, подтверждающих соблюдение установленных требований к работникам лаборатории в части подтверждения наличия у работников испытательной лаборатории (центра) опыта работы по проведению исследований в области аккредитации, указаны: трудовые или гражданско-правовые договоры или копии указанных документов.
На сегодняшний день задача подтверждения опыта персонала актуальна. Особенно, если у сотрудника большой опыт работы. Для упрощения вопроса при подтверждении можно указывать тот период времени, который необходим для соответствия работника требованиям критериев аккредитации (например, последние несколько лет) или соответствия требованиям, установленным самими лабораториями, если они не относятся к обязательной оценке соответствия и в их отношении не требуется обязательная аккредитация в национальной системе аккредитации.
Важным изменением критериев аккредитации стал уход от обязательных форм предоставления сведений о лаборатории.
Все рекомендованные образцы документов о предоставлении сведений в форме таблицы теперь заменены на перечни сведений, подтверждающих соответствие лаборатории критериям аккредитации.
Теперь таблицы, в рамках которых предоставлялись сведения, заполнять не обязательно. Можно оформлять просто перечни сведений. Это связано с развитием и расширением возможностей электронного предоставления этой информации. Кстати говоря, в ближайшем будущем всем заявителям будет дана возможность еще при подаче заявления сформировать документы в электронном машиночитаемом виде и направлять соответствующие заявления на аккредитацию.
После этого планируется подключать автоматический контроль и осуществлять электронное взаимодействие с другими федеральными органами исполнительной власти. Таким образом, при подаче заявления заявитель сможет увидеть, соответствуют ли его документы, сведения требованиям, которые установлены для него в критериях.
В каком виде сейчас оформлять перечни сведений, можно ли использовать старые формы?
Да, можно. Это удобный формат.
Поговорим об изменениях, которые необходимо внести в перечни сведений.
Изменилась формулировка, название ряда сведений без изменения сути предоставляемой информации. К ранее предоставленным сведениям добавили:
Когда разрешено законодательством, можно указывать не погрешность средства измерений, а неопределенность.
В каком случае необходимо указывать неопределенность, приписанную к конкретному средству измерения?
Ответ такой: в том случае, если методики испытаний предполагают оценку суммарной неопределенности результата, в форме, где перечисляются средства измерения, необходимо указать эту неопределенность помимо погрешности.
Сведения о результатах поверки средств измерений должны быть размещены в Федеральном информационном фонде по обеспечению единства измерений (он же - ФГИС «АРШИН»). Только после внесения сведений о результатах поверки СИ в АРШИН средства измерения можно использовать для проведения испытаний и измерений. Законодательством определены сроки внесения таких сведений в информационный фонд - до 30 рабочих дней. Если вы договоритесь с теми, кто проводит поверку средства измерения о внесении сведений ими, то можно использовать данное СИ сразу после получения из поверки. Для Росаккредитации важным является наличие соответствующих сведений в реестре.
Очень интересной особенностью является включение в состав сведений новых данных.
В состав сведений вошло: место нахождения или иная уникальная идентификация помещений.
Недостаточно указывать номер этажа и номер помещения, необходимо указывать место нахождения, чтобы избежать изменения нумерации помещений, структуры помещений. Раньше ограничивались тем, что нужна таблица такая же как на плане\схеме помещений, например из договора аренды, то теперь необходимо думать, как обозначать такие помещения.
19 апреля 2021 г. 9:11
.jpg) Записаться
Записаться
 Записаться
Записаться